Recherche
-
Syndrome cardio-rénal-métabolique (CRM) : vers un décloisonnement des maladies cardiométaboliques
-
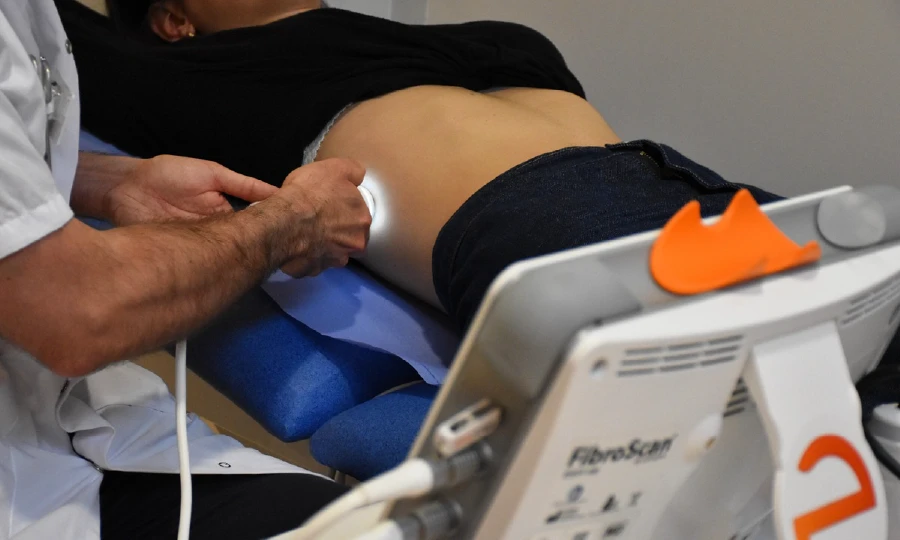
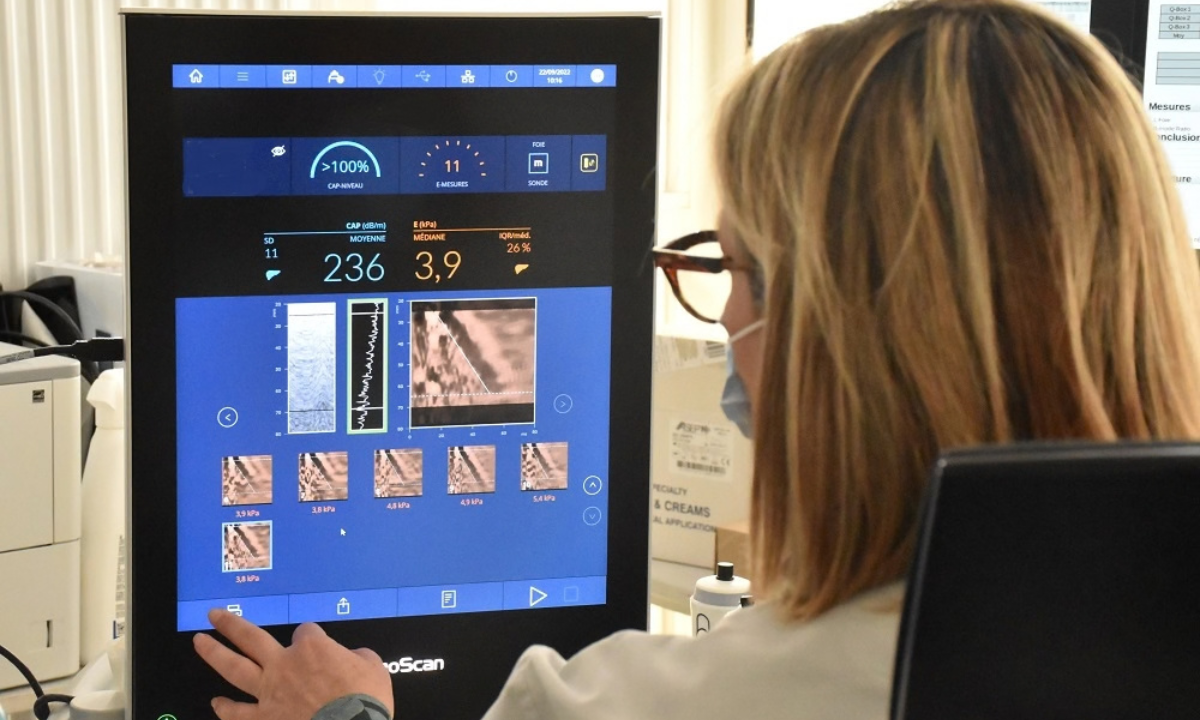
Découverte d’un nouveau biomarqueur dans le diagnostic non invasif de la MASH : la thrombospondine-2
-
Classement Clarivate 2025 : 2 chercheurs de l’IHU ICAN parmi les plus cités au monde !