La Cardiomyopathie Arythmogène du Ventricule Droit (CAVD) est la cardiomyopathie qui représente une des principales causes de mort subite chez les patients jeunes de moins de 40 ans. Elle est caractérisée par une inflammation massive du tissu cardiaque qui s’accompagne d’une perte progressive des cellules musculaires, les cardiomyocytes, qui sont remplacés par des infiltrats fibro-graisseux conduisant à un risque accru d’arythmies ventriculaires potentiellement mortelles.
Mené par le Dr Pierre Bobin, le projet CAVD vise à utiliser des pseudo-tissus cardiaques artificiels (EHT), dérivés de cellules souches pluripotentes induites humaines, en tant qu’outil de recherche translationnelle devant permettre à moyen terme de tester de nouvelles approches dans le traitement de la CAVD.

Qu’est-ce que le projet CAVD ?
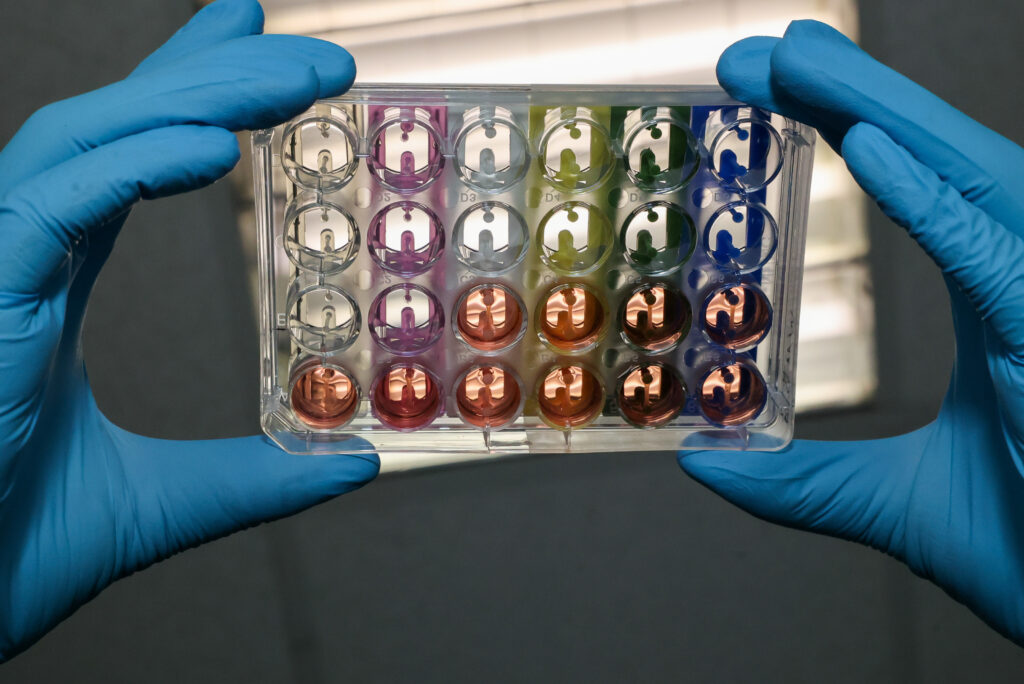
Le projet CAVD vise à développer et à améliorer la technologie des pseudo-tissus cardiaques artificiels (plus connus sous l’acronyme EHT pour Engineered Heart Tissues) dérivés de cellules souches pluripotentes induites humaines (hiPSC) afin de reconstituer in vitro un tissu cardiaque contractile mature reproduisant un stress mécanique tel qu’observé in vivo et capable de reproduire des phénotypes cellulaires et structuraux de la CAVD.
Le projet s’appuie sur des résultats préliminaires encourageants obtenus lors des trois premières années de développement de la technologie des EHT dans l’unité de recherche du Pr Estelle Gandjbakhch et du Dr Eric Villard. Il repose sur la création de lignées de cellules souches à partir de prélèvements sanguins réalisés chez des patients porteurs de mutations génétiques associées à la CAVD.
Ce projet doit ainsi permettre de développer un modèle tissulaire humain génétiquement ajustable, permettant non seulement l’observation et l’étude de la désorganisation tissulaire observée en phase terminale, mais aussi et surtout la reproduction de l’évolution de la CAVD tout au long de ses multiples phases de développement.
Le caractère innovant et unique du projet
Le développement de ce modèle, unique en France à l’heure actuelle, associé à l’utilisation de techniques et de technologies de pointe telles que l’utilisation de cellules souches iPS associée à des techniques d’édition du génome, doit permettre d’étudier les mécanismes pathologiques induits par les deux mutations majeures associées à la CAVD dans le contexte génétique du patient.
Cette nouvelle stratégie ouvre ainsi la voie à une utilisation des EHT en tant qu’outil de recherche translationnelle devant permettre à moyen terme de tester de nouvelles approches dans le traitement de la CAVD telles que la thérapie génique, avec pour horizon le développement d’une approche médicale personnalisée des pathologies cardiaques d’origine génétique.

Le mécénat au service de l’innovation
Crédit Agricole d’Ile-de-France Mécénat a accepté de soutenir ce projet de recherche innovant en 2022 et a ainsi rejoint la communauté des mécènes de l’IHU ICAN.
Dans ce cadre, nous avons eu le plaisir d’accueillir la visite de leur délégation pour une présentation du projet par l’équipe de recherche dédiée : le Pr E. Gandjbakhch (Responsable de l’unité de rythmologie de l’Institut de Cardiologie Hôpital de la Pitié-Salpêtrière), le Dr E. Villard (Responsable scientifique) et le Dr P. Bobin (Chercheur post doctorant) dans l’équipe Génomique et Physiopathologie des Maladies du Myocarde de l’UMRS 1166.
Cette rencontre a permis aux membres de la délégation de découvrir les laboratoires de recherche de l’UMRS 1166 ainsi que le laboratoire de culture cellulaire dans lequel sont développés les pseudo tissus cardiaques (EHT), modèle unique en France à l’heure actuelle.


« Le soutien de Crédit Agricole d’Ile–de–France Mécénat est important pour l’équipe, il va nous permettre d’accélérer concrètement nos travaux de recherche qui sont très couteux car il s’agit de techniques très innovantes », explique Pierre Bobin, Chercheur post-doctorant en physiologie cardiovasculaire.
Les acteurs impliqués dans le projet
Ce projet est soutenu par :
Les partenaires de ce projet :
- Le Département de Cardiologie de l’Hôpital de la Pitié Salpêtrière (AP-HP) et le Centre de référence des maladies cardiaques héréditaires ou rares de Paris (CRMR)
- ICAN BioCell-iPS
- L’UMRS 1166 (INSERM – Sorbonne Université)
- ICAN Omics metabolomics
- ICAN Omics lipidomics
- Plateforme de cytométrie







