Notre plateforme de recherche autour des maladies chroniques du foie
Les maladies chroniques du foie constituent aujourd’hui un véritable enjeu de santé publique et sont une cause majeure de décès dans le monde.
La Plateforme ICAN BioCell Human Liver Biology a pour ambition de produire des cellules hépatiques humaines primaires (hépatocytes et toutes les cellules non parenchymateuses) et de développer des modèles hépatiques en culture primaire en 2D ou 3D (tranches fines ou sphéroïdes) pour étudier les maladies chroniques du foie, en particulier la fibrose et la NASH.
Notre plateforme est accessible à toutes les unités de recherche académiques et ouverte aux projets industriels.
Vous êtes un(e) patient(e) ?
Grâce au partenariat entre l’AP-HP, l’INSERM, Sorbonne Université et l’IHU ICAN, la plateforme ICAN BioCell Human Liver Biology associe l’innovation technologique et le maintien d’une collection d’échantillons et de produits du corps humain.
Merci à tous les patients qui ont accepté de participer à la collection ICAN BioCell Human Liver Biology ! La recherche sur les maladies chronique du foie avance grâce à vous. Si vous avez fait un don pour la collection Human HepCell et que vous souhaitez vous opposer à l’une ou plusieurs recherches, vous pouvez contacter le chirurgien qui vous a opéré, ou le signaler à protection.donnees.dsi@aphp.fr.

Notre catalogue
BioCell Human Liver Biology propose un catalogue de production et vente des différents types cellulaires hépatiques :
- Hépatocytes humains (HH) frais
- Myofibroblastes hépatiques humanis (HLMF) issus de foie normal, NASH, fibrose et cirrhose
- Cellules non parenchymateuses (NPC)
- Cellules endothéliales, cellules kupffers, cellules immunes…
- Cellules biliaires issues de la vésicule biliaire
- Tranches fines de foie ou precision cut liver slices (PCLS) « sain » ou pathologique (NASH, fibrose, cirrhose). Voir la publication scientifique.
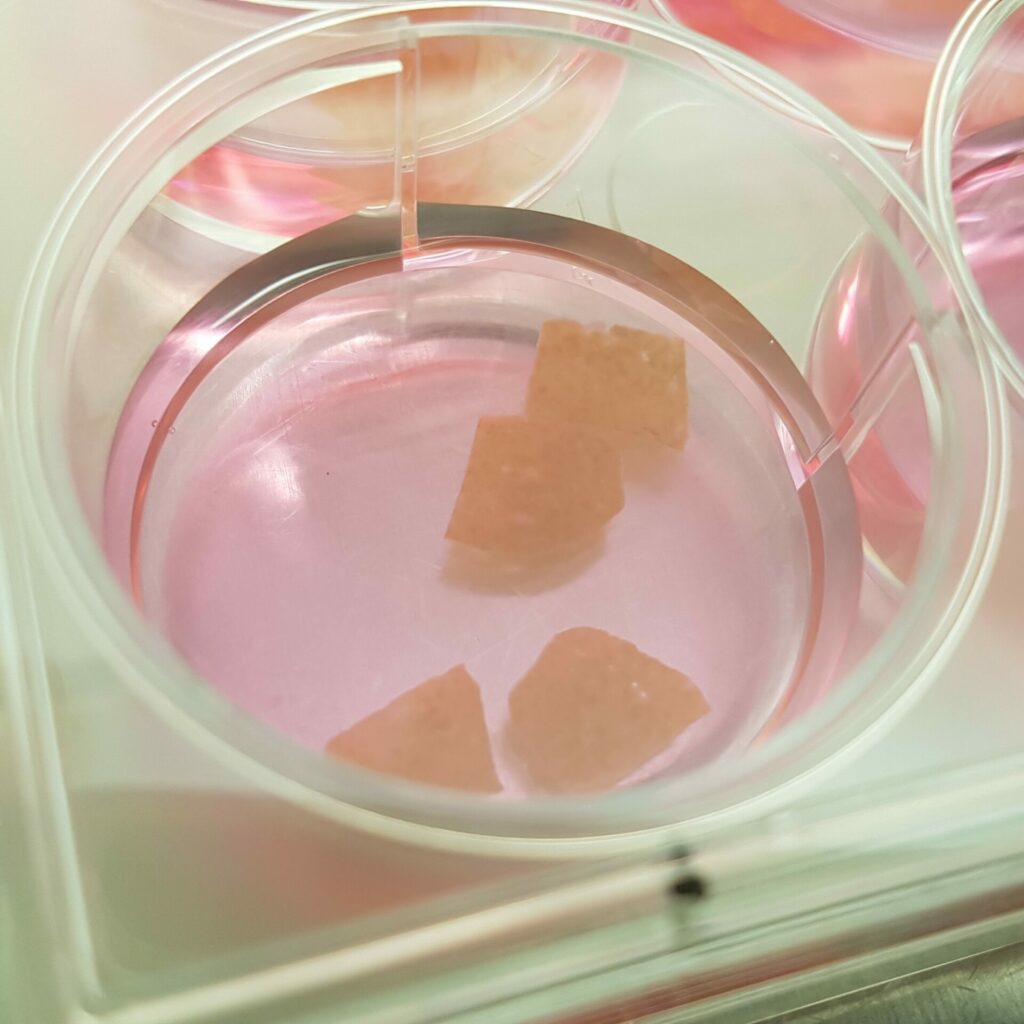
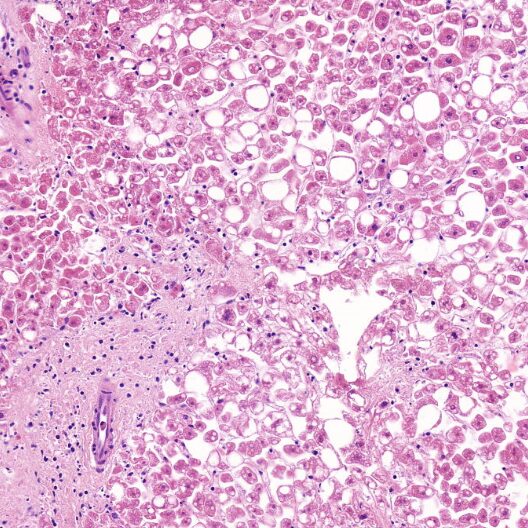
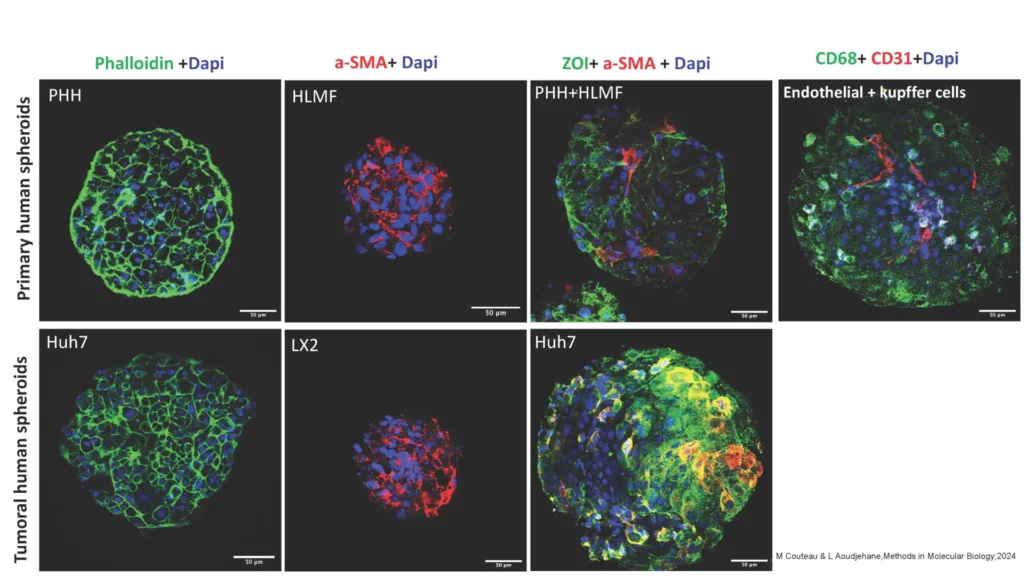
- Modèle sphéroïde/organoïde hépatique. Voir la publication scientifique.
Nos prestations de service
ICAN BioCell – Human Liver Biology propose également pour la recherche différentes prestations de service :
Fibrose
Nous avons évalué la sensibilité des myofibroblastes hépatiques issus des différents patients (normaux et cirrhotiques) aux molécules antifibrotiques à l’aide de notre plateforme Quanti-Fibrosis®. Nos données ont établi une efficacité différentielle de ces molécules révélant l’impact du polymorphisme humain et le background des maladies sur la sensibilité aux médicaments
Induction de la stéatose in vitro sur les HH ou PCLS normaux avec des acides gras.
NASH
nous disposons des modèles 2D et 3D pour étudier la stéatose hépatique associée ou non à l’inflammation
- Hépatocytes (HH) ou PCLS provenant des foies stéatosiques
- Induction de la stéatose in vitro sur les HH ou PCLS normaux avec des acides gras
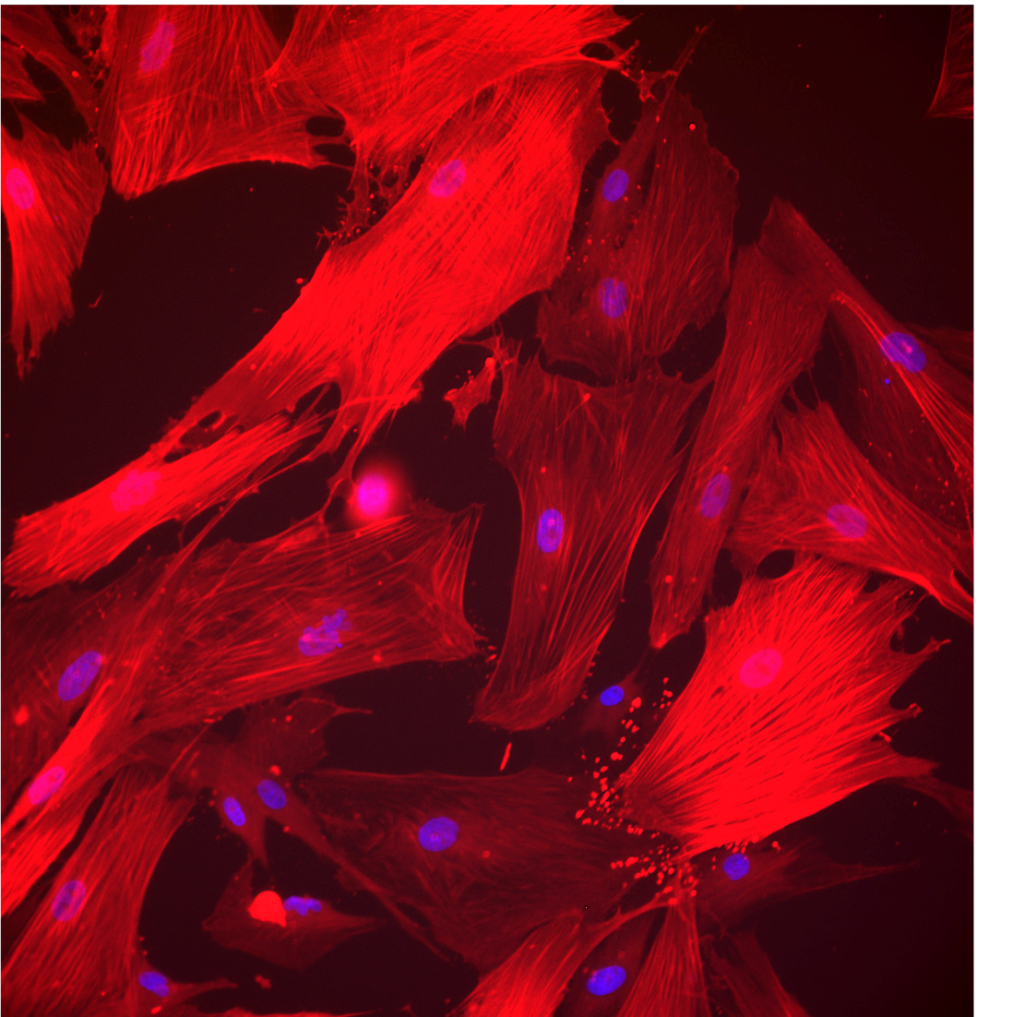
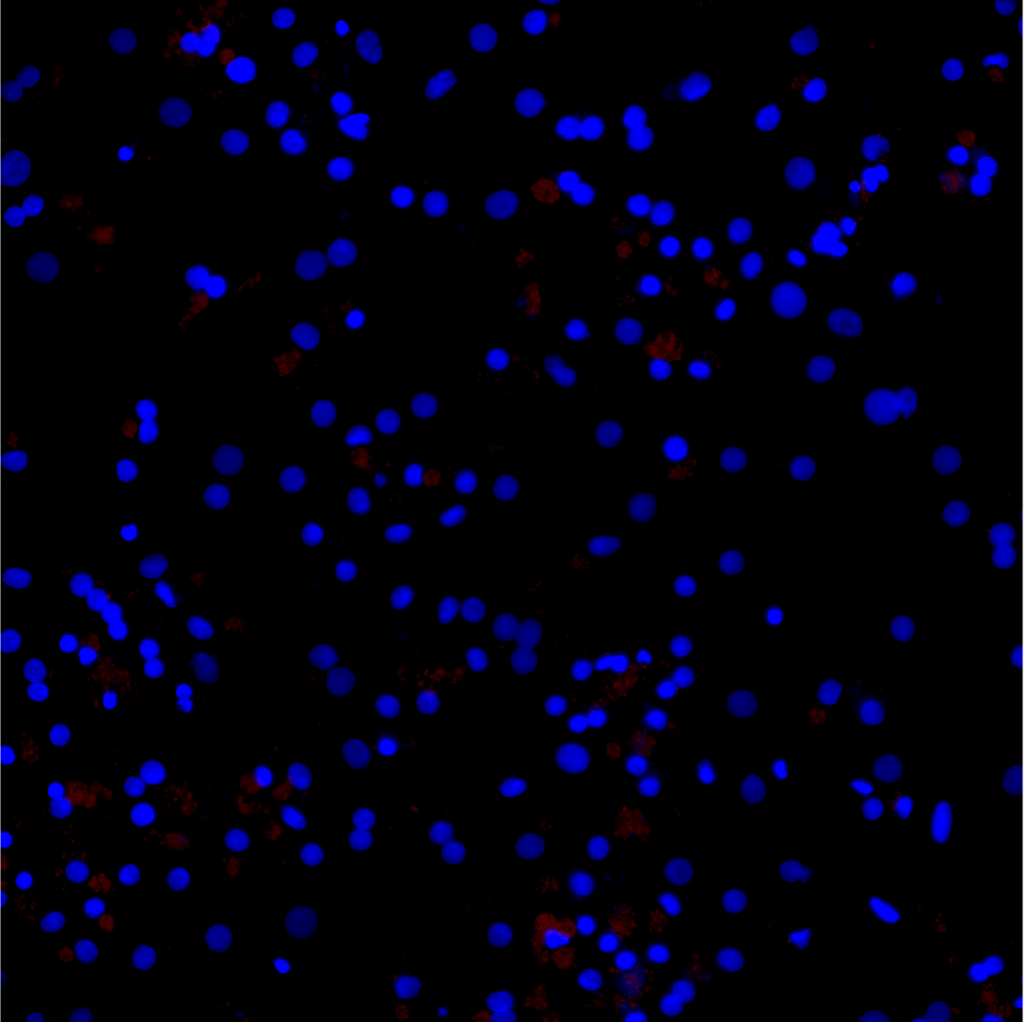
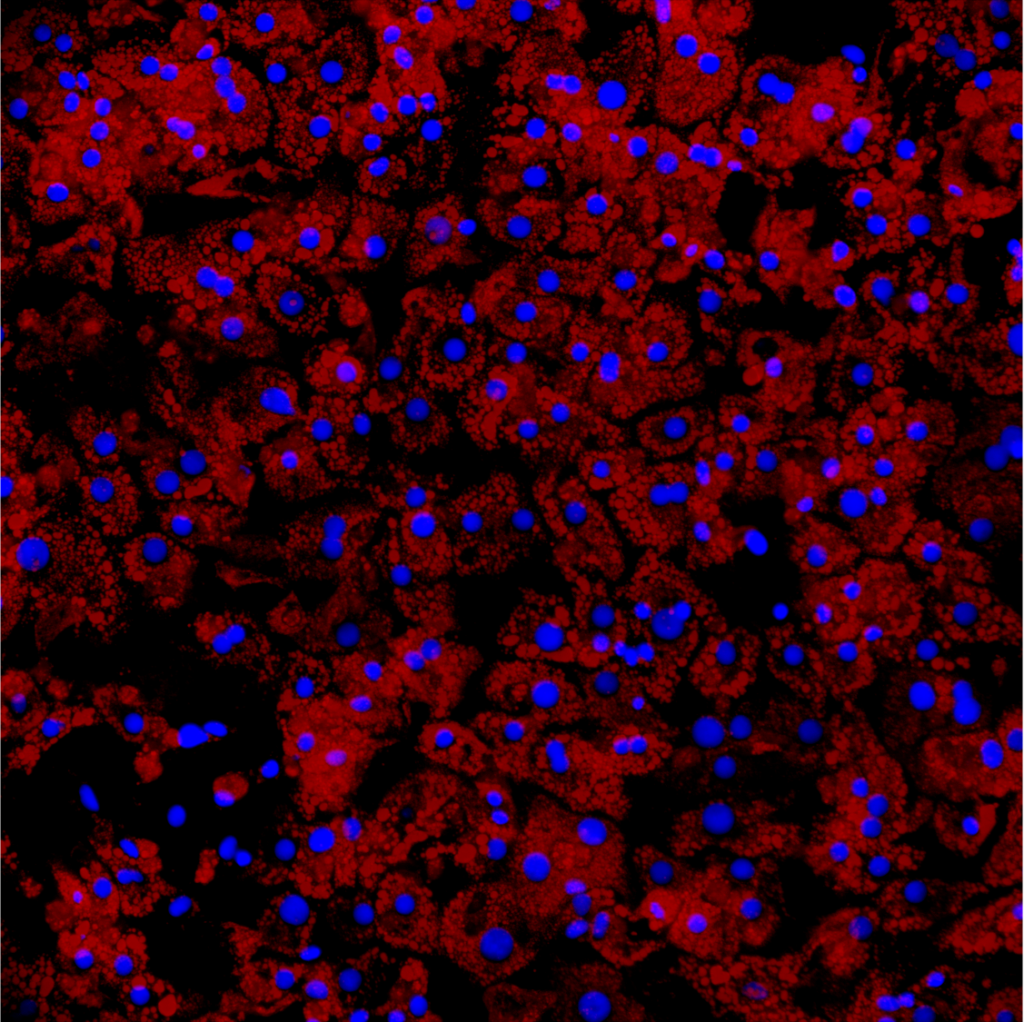
- Métabolisme lipidique (dosage des triglycérides, coloration RedOil, gènes impliqués dans le métabolisme des lipides (beta Oxydation, export des lipides, autophagie, lipogènèse…)
- Métabolisme fonctionnel hépatique (albumine, activité CYP3A4, transporteurs ABC…)
- Viabilité et toxicité (MTT, ATP et HDL) et stress oxydatif (détection de ROS), les cytokines pro-inflammatoires (QPCR et ELISA)
Conseil scientifique
- Pr Filomena Conti – Senior Scientific Advisor
- Dr Fabienne Foufelle
- Dr Laura Fouassier
- Pr Mathieu Hautefeuille
- Dr Wilfried Le Goff
- Pr Vlad Ratziu
- Pr Olivier Scatton
Contact
Lynda Aoudjehane (PhD)
Chef de projet & responsable de la plateforme
Plateforme ICAN BioCell Human Liver Biology
Faculté de Médecine de Sorbonne Université
Hôpital de la Pitié6Salpêtrière
91 boulevard de l’Hôpital
75013 Paris
Publications majeures ICAN BioCell Human Liver Biology
Zoom sur des publications majeures
06/06/2025
L’intrahepatic cholangiocarcinoma (iCCA) est une tumeur biliaire agressive où la signalisation TGF-β joue un rôle paradoxal : elle conserve un effet suppresseur sur les cellules tumorales via SMAD2/3/4, mais elle active également les fibroblastes associés au cancer (CAF), favorisant la progression tumorale et l’immunosuppression. L’inhibition directe de TGF-β (ex. galunisertib) stimule paradoxalement la prolifération tumorale, rendant cette approche contre-productive. Les auteurs démontrent que NADPH oxydase 4 (NOX4), fortement exprimée dans les CAF, collabore avec NOX1 pour médiatiser les effets pro-tumorigènes du TGF-β. L’inhibition duale NOX1/NOX4 par setanaxib réduit l’activation des CAF, diminue la fibrose tumorale et favorise l’infiltration lymphocytaire CD4+, entraînant une réduction significative de la croissance tumorale in vitro et in vivo. Cette approche offre une alternative thérapeutique plus spécifique et prometteuse que l’inhibition globale du TGF-β, avec un potentiel de combinaison avec l’immunothérapie.
06/02/2025
Les modèles cellulaires bidimensionnels (2D) utilisés classiquement pour étudier les maladies hépatiques (stéatose, fibrose, carcinome hépatocellulaire) présentent des limites car ils ne reproduisent pas fidèlement l’architecture, l’hétérogénéité cellulaire et les interactions micro-environnementales du foie. Les sphéroïdes multicellulaires tridimensionnels (3D) offrent une alternative plus physiologique, permettant d’étudier les interactions cellulaires, la progression des maladies et de tester des approches thérapeutiques. Ce protocole décrit la culture de sphéroïdes hépatiques humains à partir de cellules primaires ou de lignées cellulaires (Huh7, LX2), ainsi que l’application d’une méthode d’immunofluorescence sur sphéroïdes entiers. Les marqueurs ZO-1, α-SMA, CD68 et CD31 permettent d’identifier respectivement les hépatocytes, myofibroblastes, macrophages et cellules endothéliales. L’imagerie confocale fournit une cartographie 3D de l’organisation cellulaire, permettant une meilleure caractérisation de ces modèles biomimétiques pour la recherche translationnelle et le criblage pharmacologique.
08/2024
Cette étude préclinique valide un circuit de perfusion ex situ personnalisé permettant une transition continue et sans interruption du froid (hypothermie) vers le chaud (normothermie) pour la préservation hépatique. Le système, conçu en partenariat avec des bio-ingénieurs et adapté à une console extracorporelle LivaNova S5®, intègre un réservoir à double chambre facilitant le changement de perfusat en seulement deux minutes, sans arrêt de la perfusion. Dix foies porcins et douze foies humains écartés de la transplantation ont été perfusés durant 7 à 25 heures. Les paramètres hémodynamiques sont restés stables, aucune hyperpression n’a été observée et les lésions histologiques sont restées limitées (score de Suzuki ≤ 3). Sept foies porcins (70 %) et cinq foies humains (42 %) ont satisfait les critères de viabilité britanniques. Ce dispositif démontre la faisabilité, la sécurité et l’efficacité d’une perfusion « cold-to-warm » prolongée, surmontant les limites des systèmes commerciaux actuels et offrant de nouvelles perspectives pour l’utilisation de greffons marginaux.
07/2023
Cette revue explore les applications thérapeutiques des vésicules extracellulaires dérivées de cellules stromales mésenchymateuses (MSC-EVs) dans les pathologies hépatiques graves, notamment l’insuffisance hépatique aiguë (ALF), l’insuffisance hépatique aiguë sur chronique (ACLF), la fibrose hépatique, et la réhabilitation des greffons marginaux avant transplantation.
Les MSC présentent des propriétés anti-inflammatoires, anti-apoptotiques, antioxydantes et pro-régénératives, mais leur usage clinique est limité par des risques liés à la thérapie cellulaire (instabilité génétique, embolie, hétérogénéité de production).
Les MSC-EVs, dépourvues de noyau et riches en protéines, ARN messagers, microARN et lipides bioactifs, reproduisent les effets bénéfiques des MSC tout en contournant ces limites.
Les études précliniques montrent que les MSC-EVs atténuent la cytolyse hépatique, réduisent le stress oxydatif, inhibent l’apoptose et la ferroptose, stimulent l’autophagie et favorisent la régénération hépatique.
Dans la fibrose, elles limitent l’activation des cellules étoilées et diminuent la production de collagène. Enfin, leur utilisation lors de la perfusion normothermique de greffons hépatiques améliore la viabilité et la régénération des organes avant transplantation.
Bien qu’aucune étude clinique humaine ne soit encore disponible, ces données précliniques soutiennent le développement des MSC-EVs comme thérapie prometteuse en hépatologie régénérative et en transplantation.
29/04/2020
La transplantation hépatique (TH) est aujourd’hui le traitement reconnu des maladies hépatiques chroniques au stade terminal. Il existe actuellement une pénurie d’organes et des greffons « marginaux », en particulier stéatosiques (foie gras), sont de plus en plus utilisés pour tenter de limiter cette pénurie. La stéatose représente la principale cause de refus des greffons hépatiques par les équipes de TH car ils sont responsables de dysfonction hépatique après transplantation. L’utilisation des greffons stéatosiques pourrait réduire en partie la pénurie de greffons qui touche actuellement les patients en attente de TH. Notre stratégie est de traiter ces « candidats » greffons avant implantation à l’aide d’une perfusion normo-thermique (température physiologique 37°C) qui permettrait d’améliorer la tolérance à l’ischémie et d’extraire les vacuoles lipidiques des hépatocytes. Notre méthode de « dégraissage » consiste à agir directement sur l’accumulation excessive de lipides. Dans cette étude, nous avons imaginé un cocktail de « dégraissage » permettant de faire sortir les lipides stockés dans les hépatocytes stéatosiques. Pour cela, nous avons constitué un cocktail composé de molécules visant à activer chaque étape du métabolisme des lipides intra-hépatocytaires jusqu’à leur sortie de la cellule.
21/11/2019
La stéatose hépatique correspond à l’accumulation de graisses dans le foie. La stéatose est très fréquente (25% de la population française en est atteinte) et est très souvent associée à un surpoids et à un diabète de type 2. Souvent asymptomatique et sans conséquence, l’accumulation de graisses est responsable dans 30% des cas de lésions inflammatoires du foie (stéatohépatite non alcoolique ou NASH en anglais), pouvant aboutir à une cirrhose non-alcoolique et au cancer du foie. L’inflammation et la mort des cellules du foie dans la NASH est initialement compensée par les capacités de régénération du foie. Dans le cadre d’une agression chronique du foie, comme observé dans la NASH, ces capacités de cicatrisation sont néanmoins délétères et participent à une destruction du foie (fibrose). L’un des objectifs actuels de la recherche est d’identifier les mécanismes à l’origine de l’inflammation et de la mort cellulaire dans la NASH afin de proposer des traitements efficaces. Récemment, notre équipe a démontré grâce à des travaux réalisés chez la souris et sur des cellules de foie humain que le blocage de la mort cellulaire dans la NASH permettait de diminuer l’inflammation et la cicatrisation anormales du foie et de limiter l’accumulation des graisses dans le foie.
Toutes les publications
21/06/2023
An Efficient 5-Aminolevulinic Acid Photodynamic Therapy Treatment for Human Hepatocellular Carcinoma
10/02/2022
18/03/2021
Ex-Vivo Pharmacological Defatting of the Liver: A Review
02/03/2020
Cancer-associated fibroblasts in cholangiocarcinoma
12/10/2020
19/05/2020
28/10/2019
22/10/2019
11/08/2016
Heregulin-1ß and HER3 in hepatocellular carcinoma: status and regulation by insulin
07/03/2016
Development of an in vitro model to test antifibrotic drugs on primary human liver myofibroblasts.
27/07/2015
25/10/2013
30/04/2013
09/11/2012
10/03/2012
Epidermal growth factor receptor and HER-3 restrict cell response to sorafenib in hepatocellular carcinoma cells







